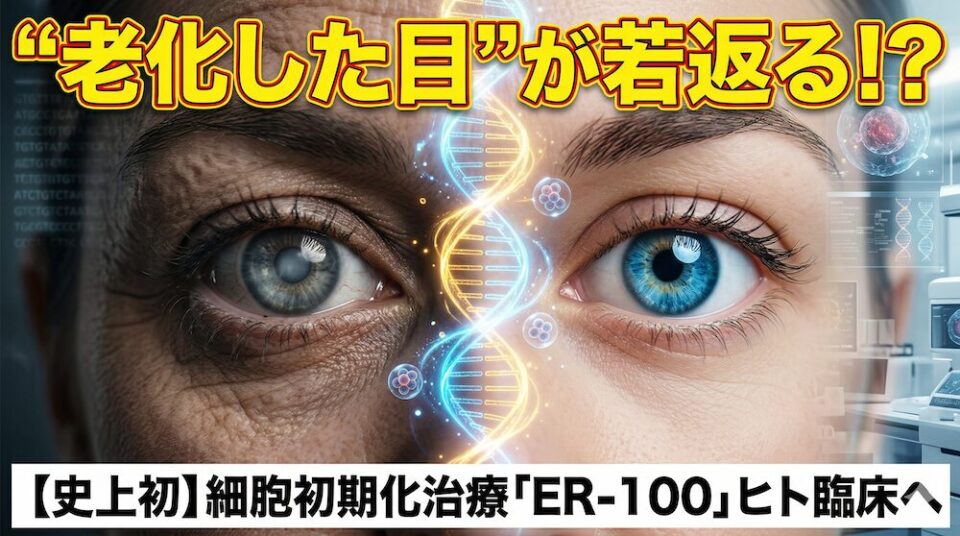
ノーベル賞の技術で"目の老化"を巻き戻す
― 史上初の若返り治療ER-100、ついにヒトへ ―
想定尺:約90分 ターゲット:一般視聴者(医療知識なしでも理解可能) トーン:知的エンタメ × 眼科医の専門的解説
■ パート1:導入・掴み(約10分)
【オープニング】
みなさん、こんにちは。眼科医の高橋です。
今日はですね、ちょっとスケールの大きい話をします。
いきなりですけど、一つ質問させてください。
「もし、老化で失われた視力が"若返って"元に戻るとしたら、信じますか?」
……いやいや、怪しいサプリの宣伝じゃないですよ。
これ、2026年1月28日に実際に起きたニュースなんです。
アメリカのFDA――日本でいう厚生労働省みたいな機関ですね――が、ある治療薬の臨床試験を正式に許可しました。その薬の名前は 「ER-100」 。
何がすごいかというと、これは 「エピジェネティック・リプログラミング」 という技術を使った、 史上初 の「細胞若返り治療」なんです。
「エピジェネティック・リプログラミング」って何? って思いますよね。
簡単にいうと、 老化した細胞を、遺伝子操作で若い状態に巻き戻す ということです。
しかもですよ、この技術のルーツをたどっていくと、日本人の研究者にたどり着きます。そう、2012年にノーベル医学・生理学賞を受賞した 山中伸弥教授 です。
山中教授が発見した「iPS細胞」の技術を応用して、マウスの目で老化を逆転させることに成功し、ついに今年、人間での臨床試験が始まった。
これが今日の話の全体像です。
【なぜ眼科医の私がこの話をするのか】
で、なんで眼科医の私がこのテーマで動画を作っているかというと、理由は単純です。
この臨床試験のターゲットが、まさに私の専門分野の疾患だから。
ER-100が最初に試されるのは、 開放隅角緑内障 と NAION(非動脈炎性前部虚血性視神経症) という2つの病気の患者さんです。
緑内障は皆さんも聞いたことがあると思います。日本人の失明原因の第1位で、40歳以上の約20人に1人がかかっている病気です。
NAIONのほうは、あまり聞き慣れないかもしれません。これは言ってみれば 「目のストローク」 ――脳卒中の目バージョンです。ある朝突然、片目の視野がガクッと欠ける。痛みはない。そして、ほとんどの場合、その視力は元に戻らない。
この2つの病気に共通するのは、 網膜神経節細胞(RGC) という細胞が死んでいくことです。RGCは目と脳をつなぐケーブルの大元になる細胞で、一度死んだら再生しない。少なくとも、今まではそう考えられてきました。
ER-100は、この「一度死んだら戻らない」という常識を覆そうとしている。
眼科医として、これは無視できないニュースです。今日は、この話を科学的にきちんと解説しつつ、過度な期待は禁物であるということも含めて、正直にお話しします。
■ パート2:そもそも「老化」とは何か(約12分)
【DNAは設計図、でもそれだけじゃない】
さて、ER-100の話に入る前に、まず 「そもそも老化って何なの?」 という根本的な疑問を整理させてください。
私たちの体は約37兆個の細胞でできています。で、すべての細胞は基本的に同じDNAを持っている。皮膚の細胞も、肝臓の細胞も、網膜の神経細胞も、設計図は全部同じなんです。
じゃあ、なんで皮膚細胞と神経細胞はまったく違う見た目で、まったく違う仕事をしているのか。
答えは 「エピジェネティクス」 にあります。
「エピ」はギリシャ語で「上に」という意味。つまり、 DNAという設計図の"上に"書き込まれた追加の情報 のことです。
たとえ話で説明しますね。
DNAを「料理のレシピ本」だと思ってください。全ページに膨大なレシピが書いてある。でも、皮膚細胞は「第3章 皮膚の作り方」のページだけ開いていて、残りのページには付箋が貼ってあって「このページは読まないで」となっている。神経細胞は別のページが開いている。
この 「どのページを開くか、どのページを閉じるか」を決める仕組み がエピジェネティクスです。
具体的には、DNAに メチル基(-CH₃) という小さな化学タグがくっつくことで、「この遺伝子はオフ」「この遺伝子はオン」というスイッチが制御されています。これを 「DNAメチル化」 といいます。
【老化=エピジェネティックな情報の劣化】
ここからが重要です。
年を取ると、このメチル化のパターンが だんだん崩れていく んです。
本来オフであるべき遺伝子がオンになったり、オンであるべき遺伝子がオフになったりする。レシピ本でいえば、付箋がポロポロ剥がれたり、変なページに付箋が貼られたりして、どのレシピを使えばいいのか細胞が混乱してくる。
これが 「エピジェネティック・ノイズ」 と呼ばれる現象で、ハーバード大学の デビッド・シンクレア教授 は、これこそが 老化の根本原因 だと主張しています。
シンクレア教授の理論は 「老化の情報理論(Information Theory of Aging)」 と呼ばれていて、こういう考え方です。
「老化とは、細胞が持っている"若い頃の設計情報"が、ノイズによって読めなくなっていくプロセスである」
ここでもう一つ、わかりやすいたとえを出しましょう。
CDって覚えてますか? 今はストリーミングの時代ですけど、CDって傷がつくと音飛びしますよね。でも、CDの表面に傷がついても、 CDに焼き込まれた元の曲データ自体は消えていない 。傷を修復できれば、また元通りの音楽が再生できる。
シンクレア教授は、 細胞の老化も同じだ と言っているわけです。エピジェネティックな「傷」が蓄積して細胞の機能が低下しているだけで、若い頃の情報のバックアップは細胞の中にまだ残っている。だったら、そのバックアップにアクセスして、エピジェネティクスを若い状態にリセットできれば、細胞は若返るはずだ、と。
【メチル化時計——老化を数値化する】
ちなみに、このDNAメチル化パターンの変化を使って、生物学的な年齢を計算する方法があります。 「ホルバス時計(Horvath Clock)」 あるいは 「エピジェネティック・クロック」 と呼ばれるものです。
UCLA(カリフォルニア大学ロサンゼルス校)のスティーブ・ホルバス教授が開発したもので、DNAのメチル化パターンを分析すると、実年齢とは関係なく、その細胞が「生物学的に何歳か」がわかる。
たとえば、実年齢60歳の人でも、生活習慣が良ければ生物学的年齢は50歳かもしれないし、不摂生していれば70歳かもしれない。
この時計が重要なのは、 老化を「数値」として測れる ということです。もし若返り治療をやったとき、メチル化時計が逆方向に動いたら、それは「細胞が若返った」客観的な証拠になる。
実際、ER-100のもとになったマウス実験では、このメチル化時計が 若い方向に巻き戻った ことが確認されています。
■ パート3:山中因子とiPS細胞——ノーベル賞の原点(約12分)
【一人の整形外科研修医の転身】
さて、いよいよ今日の話の出発点、山中伸弥教授の話をしましょう。
山中先生のキャリアは、実は整形外科の研修医から始まっています。1987年に神戸大学を卒業して、最初は整形外科医として手術をしていた。
ところが、研修医時代に自分の不器用さに絶望して、「俺は臨床じゃなくて基礎研究に向いているんじゃないか」と思い始める。奥様には「ちゃんと臨床医をやりなさい」と言われたそうですが、結局、奈良先端科学技術大学院大学のポジションに応募して、基礎研究の道に進みました。
この決断がなければ、iPS細胞は生まれていなかったし、今日のER-100もなかったかもしれません。
【2006年の大発見:4つの遺伝子で細胞が初期化できる】
山中先生が注目したのは、 「分化した大人の細胞を、受精卵に近い状態に戻すことはできないか?」 という問いでした。
当時の常識では、「細胞の分化は一方通行」と考えられていました。皮膚細胞は皮膚細胞のままで、もう他の細胞にはなれない、と。
しかし山中先生のチームは、24個の候補遺伝子の中から試行錯誤を重ね、最終的に たった4つの遺伝子 を細胞に導入するだけで、大人の皮膚細胞を受精卵に近い「万能細胞」に変えられることを発見しました。
その4つの遺伝子が作るタンパク質が、いわゆる 「山中因子」 です。
- Oct4(Oct3/4)
- Sox2
- Klf4
- c-Myc
頭文字をとって 「OSKM」 と呼ばれます。
この技術で作られた万能細胞が 「iPS細胞(人工多能性幹細胞)」 。2006年にマウスで、2007年にはヒトの細胞でも成功が報告されました。
これがどれだけ衝撃的だったかというと、John Gurdon博士(1962年にカエルの核移植実験で細胞の初期化が可能であることを示した研究者)と共に、2012年のノーベル医学・生理学賞を受賞しています。授賞理由は 「成熟した細胞が多能性を持つように再プログラミングできることの発見」 。
日本人として本当に誇らしい業績ですよね。
【iPS細胞の「2つの問題」】
ただし、この素晴らしいiPS細胞技術には、治療応用を考える上で2つの大きな問題がありました。
問題①:腫瘍リスク
4つの山中因子のうち、 c-Myc は実は がん遺伝子(オンコジーン) なんです。つまり、細胞を若返らせる力はあるけど、同時にがんを引き起こすリスクがある。実際にマウス実験では、4因子を全部使うと「テラトーマ」と呼ばれる醜い腫瘍ができることがありました。
問題②:アイデンティティの消失
4因子でフルに初期化すると、細胞が完全にリセットされて、「私は皮膚細胞です」「私は神経細胞です」という 細胞のアイデンティティが失われてしまう 。これは体の中でやったら大変なことになります。網膜の神経細胞が急に「何の細胞だったっけ?」となったら、目として機能しなくなる。
つまり、iPS細胞技術をそのまま体の中で使うのは 「危険」 だったんです。
若返らせたいけど、細胞の種類を変えてしまいたくはない。もっと「ほどほど」にリプログラミングする方法はないのか。
ここで登場するのが、デビッド・シンクレア教授のチームです。
■ パート4:シンクレア研究室の大逆転——マウスの視力が回復した(約15分)
【「c-Mycを抜いてみよう」——誰も信じなかった実験】
ハーバード大学のデビッド・シンクレア教授の研究室で、大学院生のユアンチェン・ルー博士が、ある大胆な実験を提案しました。
「4つの山中因子のうち、がん遺伝子のc-Mycを除いた3つだけ――OCT4、SOX2、KLF4(OSK)――で実験してみたらどうだろう?」
当時の学界の常識では、「4つ全部必要」というのがコンセンサスでした。なにせノーベル賞をもらった研究でそう示されているわけですから、3つに減らしたら効果がなくなるだろう、と皆が思っていた。
シンクレア教授自身も後にこう語っています。
「4つ全部が必要だというのが定説だった。ノーベル賞を受賞した研究でそう示されていたら、普通はそれを信じる。世界中で誰一人として、3つだけで効果があるとは思わなかった。でも、やってみるまではわからない」
【2020年、Natureの表紙を飾った実験】
結果は驚異的でした。
2020年12月2日、科学誌Natureの 表紙 を飾った論文で、シンクレアチームは以下の成果を報告しました。
まず、彼らはAAV(アデノ随伴ウイルス)というウイルスベクターを使って、マウスの網膜神経節細胞にOSKの3遺伝子を導入しました。ウイルスといっても、人体にはほぼ無害な遺伝子の「運び屋」です。
実験①:視神経挫滅モデル
マウスの視神経をわざと圧挫して損傷させた後、OSKを導入。結果、OSKを発現させたマウスでは、生き残った網膜神経節細胞の数が 2倍 に増え、視神経の軸索再生が 5倍 に増加しました。
普通、大人の哺乳類では、視神経は一度損傷したら再生しません。それが、3つの遺伝子を入れるだけで、生まれ変わったように再生を始めた。
実験②:緑内障モデル
マウスで人工的に緑内障を起こし、視力が低下した状態でOSKを投与。すると、低下していた視力が 回復 しました。緑内障で失われた視力が戻った、というのは 史上初 の報告です。
実験③:加齢マウスの視力回復
12か月齢の老齢マウス(人間でいうと50〜60歳くらい)にOSKを投与。加齢で自然に低下していた視機能が、 若いマウスのレベルに近づいた 。
【何が起きていたのか?——「部分的リプログラミング」の正体】
ここで重要なのは、OSKの3因子でリプログラミングしたとき、細胞に何が起きていたかです。
まず、 メチル化時計が若い方向に巻き戻った 。老化した網膜神経節細胞のDNAメチル化パターンが、若い細胞のパターンに近づいていました。
次に、 遺伝子の発現パターンも若返っていた 。老化で変化していた約464個の遺伝子の発現パターンが、OSK処理によって若い状態に戻されたことが確認されました。
しかし——ここがポイントなんですが—— 細胞のアイデンティティは失われなかった 。網膜神経節細胞はちゃんと網膜神経節細胞のままで、幹細胞に戻ったりはしなかった。
なぜか? c-Mycを抜いたからです。
c-Mycは「アクセル全開」で細胞を初期化まで持っていくドライバーのような存在で、これがないと細胞は完全な初期化にまでは到達できない。でも、老化に伴うエピジェネティックなノイズを取り除いて、若い状態のメチル化パターンを回復させるには十分 だった。
シンクレア教授はこう表現しています。
「細胞は若い頃のエピジェネティック情報のバックアップを保持している。OSKはそのバックアップにアクセスして、CDの傷を修復するようなものだ」
【TET1/TET2という「修復装置」】
さらに興味深いのは、このプロセスが TET1 と TET2 という酵素に依存していたことです。
TET1/TET2は、DNAからメチル基を取り除く「脱メチル化酵素」です。つまり、OSKが命令を出して、TET1/TET2が実際にDNAの上の余計なメチル化マークを消していく、というメカニズムが働いていた。
実験では、TET1またはTET2の機能を阻害すると、OSKによる視力回復効果が消失しました。これは、この若返りプロセスが「積極的なDNA脱メチル化」を必要としていることの強い証拠です。
【この論文の衝撃】
この2020年のNature論文は、科学界に巨大なインパクトを与えました。
Nature Reviews Genetics誌は「Hitting reverse on ageing(老化にリバースをかける)」というタイトルで紹介記事を出し、Nature Reviews Neuroscience誌も「Retinal rejuvenation(網膜の若返り)」として取り上げています。
何がそんなに衝撃的だったかというと、3つの遺伝子を入れるという比較的シンプルな操作で、生きた動物の複雑な組織において安全に老化を逆転できたこと。これは世界初の実証でした。
そして、この研究の延長線上にあるのが、今回のER-100なんです。
■ パート5:ER-100臨床試験——いよいよ人間で試される(約15分)
【Life Biosciences社とは】
ER-100を開発しているのは、ボストンに本社を置く Life Biosciences社 です。シンクレア教授が共同創業に関わっている会社で、2017年の設立以来、累計で1億5800万ドル(約230億円)以上の資金を調達しています。
会社のミッションは明確で、 「部分的エピジェネティックリプログラミング(PER)技術を使って、加齢性疾患を逆転・予防する」 こと。
【マウスからサルへ——非ヒト霊長類での確認】
人間での臨床試験に入るためには、マウスでの成功だけでは不十分です。もっと人間に近い動物で安全性と効果を確認する必要がある。
Life Biosciences社は、 非ヒト霊長類(サル) で広範な前臨床試験を行いました。
サルの目にNAION様の視神経障害を人工的に誘発し、ER-100(OSKを発現するAAVベクター)を硝子体内注射で投与。結果は以下の通りです。
- OSKの発現が確認された :免疫組織化学的に、投与された目の網膜細胞でOCT4、SOX2、KLF4の発現が確認された
- 視機能の改善 :パターンERG(PERG)の応答が有意に改善した。PERGは網膜神経節細胞の機能を反映する電気生理学的検査です
- 軸索密度の維持 :視神経の軸索密度が、治療群で有意に保たれていた
- メチル化パターンの回復 :DNAメチル化の解析で、神経再生に関連するプロセスの機能的エンリッチメントが確認された
- 予防モデルと救済モデルの両方で有効 :障害の前に投与しても、後に投与しても効果があった
これらのデータが、2024年のアメリカ眼科学会(AAO)年次総会で発表されています。
【Phase 1試験の設計】
そして2026年1月28日、FDAがER-100のIND(治験薬)申請を正式に承認。臨床試験登録番号は NCT07290244 。
この試験のポイントを整理しましょう。
対象患者:
- 開放隅角緑内障(OAG)の患者
- 非動脈炎性前部虚血性視神経症(NAION)の患者
投与方法: ER-100は硝子体内注射で投与されます。つまり、目の中にAAVベクターを直接注入する。これに加えて、 ドキシサイクリン (抗生物質)を全身投与します。
なぜドキシサイクリンが必要かというと、ER-100は「誘導型発現システム」を使っているからです。AAVベクターで細胞にOSKの遺伝子を入れますが、ドキシサイクリンを飲んでいる間だけOSKが発現する仕組みになっている。つまり、OSKの「スイッチのオンオフ」を外部からコントロールできる。
これは安全性の観点から非常に重要です。もし何か問題が起きたら、ドキシサイクリンの投与を止めれば、OSKの発現も止まる。
OSK発現期間: 8週間
Life Biosciences社の最高科学責任者であるシャロン・ローゼンツワイグ-リプソン博士によると、マウスのデータでは8週間だけでなく、3か月、あるいはそれ以上の期間でも安全にリプログラミングと安全性が確認されているとのことです。
主要評価項目:
- 安全性
- 忍容性
- 免疫反応
副次評価項目:
- 各種視機能評価(視力、視野など)
Phase 1試験なので、主な目的は 「安全に使えるかどうか」 の確認です。効果の証明は、その先のPhase 2、Phase 3に委ねられます。
【なぜ「目」が最初のターゲットなのか——眼科医としての解説】
ここは眼科医として少し専門的な解説をさせてください。
「なぜ若返り治療の最初のターゲットが脳でも心臓でもなく、目なのか」という疑問を持つ方もいると思います。実はこれ、非常に合理的な理由があるんです。
理由①:免疫特権部位である
目の内部(特に硝子体腔や前房)は 「免疫特権部位」 と呼ばれていて、通常の免疫反応が抑制されている場所です。AAVベクターのような外来物質を入れても、全身投与に比べて免疫反応が起きにくい。これは安全性の面で大きなアドバンテージです。
理由②:局所投与が可能
硝子体内注射という確立された投与経路があります。眼科では加齢黄斑変性の治療などで、硝子体内注射は日常的に行われている手技です。全身に薬を回す必要がなく、ターゲットの細胞に直接届けられる。
理由③:客観的な評価指標がある
視力、視野、OCT(光干渉断層計)、PERG(パターン網膜電図)など、治療効果を 数値で客観的に測定できる 手段が豊富に揃っている。「なんとなく若返った気がする」ではなく、ちゃんと数字で示せる。
理由④:網膜神経節細胞はCNS(中枢神経系)の一部
これがちょっとマニアックだけど大事な話です。網膜は発生学的に脳の一部なんです。つまり、網膜神経節細胞のリプログラミングに成功すれば、 脳の神経細胞にも応用できる可能性 が開ける。目は「脳への窓」であり、若返り治療の最初の実験場として最適なんです。
【NAIONという疾患の深刻さ】
もう少しNAIONについて掘り下げさせてください。
NAIONは、50歳以上の成人における最も一般的な急性視神経障害です。アメリカでは年間3万件以上が発生しています。
症状は典型的で、 ある朝突然、片目の視野が欠ける 。多くの場合、上半分か下半分がグレーアウトします。痛みはありません。
そして恐ろしいのは、 現在、NAIONには承認された治療法が一つもない ということです。
実は以前、QPI-1007という薬の大規模な臨床試験(Phase 2/3)が行われました。これはカスパーゼ2というアポトーシス(細胞死)関連タンパク質を標的としたsiRNA(小さな干渉RNA)で、NAION発症後の急性期に硝子体内注射で投与するものでした。725人の患者が参加した大規模試験でしたが、 主要評価項目を達成できませんでした 。
また、Oculis社が開発しているPrivosegtor(プリボセグトール)という神経保護薬も、NAION向けのPIONEER-3試験を2026年半ばに開始予定ですが、まだ結果は出ていません。
つまり、NAIONは12件以上の治療法が試されてきたにもかかわらず、 どれも有効性を証明できていない という、医学的に非常に手ごわい疾患なんです。
さらに深刻なのは、NAION患者の 60%以上が永続的な視覚障害 を残すこと、そして 2〜3年以内に反対側の目にも発症する確率が15〜30%ある こと。
これだけの未充足医療ニーズ(アンメット・メディカル・ニーズ)がある疾患に対して、まったく新しいアプローチとしてエピジェネティックリプログラミングが挑む。これは本当に注目に値するチャレンジです。
■ パート6:シンクレアの光と影——科学者として正直に語る(約15分)
【ここからは「影」の話をします】
さて、ここまでER-100のワクワクする話をしてきましたが、科学的に誠実であるために、 デビッド・シンクレア教授という研究者の評価について、批判的な側面もきちんとお話しします 。
これをやるかどうか迷ったんですが、やっぱり視聴者の皆さんに正確な情報を提供するのが私の役割だと思うので、避けずに話します。
【レスベラトロール事件——7億2000万ドルの教訓】
シンクレア教授が世界的に有名になったのは、実はER-100より遥か前の、2003年の研究がきっかけでした。
彼のチームは、赤ワインに含まれるポリフェノールの一種 レスベラトロール が、 サーチュイン(SIRT1) という酵素を活性化し、長寿効果があると報告しました。
「赤ワインが体に良い」というフランス・パラドックスの謎が科学的に説明できた、として世界中で大ニュースになりました。シンクレア教授はレスベラトロールについて非常に楽観的な発言をし、メディアも大きく取り上げた。
この研究をもとに設立されたのが Sirtris Pharmaceuticals という会社で、2008年に製薬大手のGlaxoSmithKline(GSK)が 7億2000万ドル(当時のレートで約700億円) で買収しました。
ところが。
その後の研究で、 レスベラトロールがサーチュインを直接活性化するという結論は、アッセイ(測定法)のアーティファクト(人工的な誤り)だった ことが明らかになりました。使われていた蛍光プローブがレスベラトロールと非特異的に反応していたのです。
GSKはSirtrisのレスベラトロール誘導体SRT501の臨床試験を安全性の懸念から中止し、2013年にはSirtrisを完全に閉鎖しました。7億2000万ドルの投資は、基本的に水の泡になった。
これは製薬業界では 「科学的ハイプの教訓」 として語り継がれている事例です。
【サーチュイン・長寿遺伝子論争】
レスベラトロール問題はサーチュイン全体の信頼性にも波及しました。
シンクレア教授は著書『LIFESPAN(老いなき世界)』(2019年、ニューヨーク・タイムズのベストセラー11位)で、サーチュインが酵母からヒトまで保存された長寿遺伝子であり、NMNやレスベラトロールでその活性を高めれば老化を防げると主張しています。
これに対して、City of Hope National Medical CenterのCharles Brenner教授が2023年にArchives of Gerontology and Geriatricsに痛烈な書評を発表しました。
Brenner教授の批判のポイントはこうです。
- 酵母のサーチュイン遺伝子SIR2は、一つの老化モデルでは500万個の細胞のうち1個だけに寿命延長効果があるが、培養全体としてはむしろ寿命を短縮する
- 線虫やショウジョウバエでのサーチュインによる寿命延長は、2011年に7機関の共同研究で独立に再現できなかったと報告されている
- レスベラトロールがサーチュイン活性化剤でないことは2005年時点で明らかだったにもかかわらず、シンクレア教授は今なおレスベラトロールを支持している
率直に言って、これはかなり厳しい批判です。
【2023年Cell論文への疑問】
2023年1月、シンクレア研究室はCell誌に「老化の情報理論」を支持する論文を発表しました。山中因子を使ってマウスの老化をある程度制御できることを示す内容でした。
しかし、この論文にもフォーマルな反論が寄せられています。反論者が指摘したのは、実験で使われた処理がp53依存的な細胞死を30日以内に引き起こすことが知られているのに、その期間中のマウスの観察が行われていない、という点でした。
【2024年のアカデミー辞任事件】
さらに2024年には、シンクレア教授が共同創設した Academy for Health and Lifespan Research の会長を辞任しています。きっかけは、彼の兄弟が関わるAnimal Bioscience社が「犬用サプリメントが老化を逆転させた」と主張したことで、アカデミーの他のメンバーが次々と辞任する「カスケード」が起きたためです。
ウォール・ストリート・ジャーナルがこの騒動を報じています。
【それでもER-100は別物——なぜ注目に値するのか】
——さて、ここまでシンクレア教授の過去の問題をかなり率直に話しました。
「じゃあER-100も信用できないんじゃないの?」
と思う方もいるかもしれません。その疑問は正当です。
でも、私は以下の理由で、ER-100は過去のレスベラトロールやNMNとは質的に異なると考えています。
第一に、2020年のNature論文は現在まで撤回されておらず、独立したグループによる検証も進んでいます。 シンクレア教授の論文の中で、レスベラトロール関連の論文は一つも撤回されていないものの信頼性に疑問が呈されている。しかしOSKリプログラミングの研究は、その後のフィールド全体の発展を見ても、基本的な知見が再現されています。
第二に、FDAがIND申請を承認した。 これは何を意味するかというと、FDAが前臨床データ(マウス+サル)を精査した上で、「ヒトで試験を行っても安全性の観点から妥当」と判断した、ということです。Life Biosciences社のCSOによると、FDAとの対話は約2年前から行われており、毒性試験、分布試験、臨床計画について協議を重ねた結果の承認だそうです。
第三に、今回はPhase 1のRCT(ランダム化比較試験)です。 サプリメントの宣伝やマウス実験の拡大解釈とは違い、厳格な規制のもとで行われるヒト臨床試験です。結果は良くても悪くても、透明に報告されます。
科学は人で判断するものではなく、データで判断するものです。シンクレア教授に対する批判は科学界では正当なものが多いですが、ER-100については 「データが出てから判断する」 というのが最も科学的な態度だと思います。
■ パート7:若返り治療の未来——競合企業と展望(約11分)
【リプログラミング企業の「群雄割拠」】
ER-100は最初にヒト臨床試験に到達したリプログラミング治療ですが、この分野で研究開発を進めている企業は他にも複数あります。まさに群雄割拠の状態です。
Altos Labs(アルトス・ラボ)
2022年に設立されて、初期資金が 30億ドル(約4500億円) 。Amazon創業者のジェフ・ベゾスが主要投資家の一人と報じられています。山中伸弥教授が科学アドバイザリーボードの議長を務めているのも注目です。
Altos Labsの創設科学者であるフアン・カルロス・イスピスア・ベルモンテ博士は、2016年に早老症マウスでの部分的リプログラミングによる寿命延長を発表した人物で、この分野のパイオニアの一人です。
2024年にはScience Translational Medicineに、部分的細胞リプログラミングがマウスの寿命を延長し健康指標を改善したというデータを発表しています。ただし、腫瘍リスクの増加も同時に報告されており、安全性の課題がまだ残っています。
2025年10月にはCell誌に、特定の遺伝子をオフにすることで細胞のドリフトを防ぎ、より若く制御された状態を回復できるという新しいデータを出しています。
YouthBio Therapeutics(ユースバイオ)
こちらは 脳 をターゲットにしている会社です。主力候補のYB002は、アルツハイマー病に対する部分的リプログラミング遺伝子治療。2025年9月にはFDAとのINTERACT会議を完了し、前臨床データがバイオ活性を示すことをFDAが認めたと発表しています。
CEOのユーリ・デイギン氏は、Life Biosciences社のER-100のFDA承認を受けて、こう述べています。「これは部分的リプログラミング分野全体にとって大きなマイルストーンだ。FDAがこのアプローチに対して前向きで先進的な姿勢を示していることと一致する」
ヒト臨床試験の開始は約3年後を目標としています。
Turn Biotechnologies(ターンバイオ)
スタンフォード大学のヴィットリオ・セバスティアーノ教授が共同創業した会社で、mRNAベースのアプローチを取っています。AAVウイルスではなく、mRNAで山中因子(4因子+LIN28とNANOGの計6因子)を一時的に発現させる方法です。20種類以上のヒト細胞で若返り効果を確認していると報告しています。
Retro Biosciences
OpenAIのサム・アルトマン氏が出資している会社で、血漿希釈アプローチなど、独自の若返り戦略を追求しています。
【なぜ今、この分野が爆発的に動いているのか】
ここ数年でリプログラミング分野に数十億ドル規模の投資が流れ込んでいる背景には、いくつかの要因があります。
- 2020年のSinclair Nature論文で「部分的リプログラミングの原理証明」が示された
- エピジェネティック・クロックという定量的な「若返り測定ツール」が確立された
- AAVベースの遺伝子治療の安全性データが他の領域(網膜ジストロフィーのLuxturnaなど)で蓄積された
- AI/機械学習の発展により、リプログラミング効率の最適化が加速している
そして、2026年のER-100 Phase 1開始は、この分野全体にとって 「概念実証」のフェーズに入った ことを意味します。
【眼科の未来——パラダイムシフトの可能性】
最後に、眼科医としての私の考えを述べさせてください。
現在の眼科治療は、緑内障にしてもNAIONにしても、基本的に 「これ以上悪くならないようにする」 治療です。緑内障なら眼圧を下げて進行を遅らせる。NAIONに至っては、それすらできない。
もしER-100が安全で、しかも効果があることが証明されたら、眼科は 「失われた機能を回復させる」 治療の時代に入ります。
これは パラダイムシフト です。「治療できない」から「若返らせる」への転換。
もちろん、Phase 1はあくまで安全性確認が目的で、結果が出るのは 早くても2026年末から2027年初め の見通しです。Phase 2、Phase 3と進んで、実際に患者さんに使えるようになるまでには、おそらくさらに5〜10年はかかるでしょう。
でも、 歴史的に見て、今この瞬間が「始まりの始まり」であることは間違いない と私は思います。
■ エンディング(約5分)
【まとめ】
今日の話を振り返りましょう。
2006年、京都大学の山中伸弥教授が4つの遺伝子で細胞を初期化できることを発見した。
2020年、ハーバード大学のシンクレア教授のチームが、そのうち3つの遺伝子だけで、マウスの老化した目を若返らせることに成功した。
そして2026年1月、この技術を使った治療薬ER-100が、FDAの承認を得て史上初のヒト臨床試験に入った。
山中因子 → OSKリプログラミング → ER-100 → ヒト臨床試験。
20年の歳月をかけて、ノーベル賞の発見が実際の治療法として人間の目に届こうとしている。
【科学リテラシーとしての正しい距離感】
ただし、繰り返しになりますが、大事なことを最後にもう一度言わせてください。
ER-100はまだPhase 1です。 安全性の確認が主目的で、効果が証明されたわけではありません。
シンクレア教授は過去にレスベラトロールやサーチュインの研究で誇張があったと批判されている研究者でもあります。
だからこそ、今回のPhase 1の結果は重要です。厳格な臨床試験の枠組みの中で、初めてこの技術がヒトで検証される。
結果が良ければ、人類の医学史に残るブレークスルーになります。結果が悪くても、科学は確実に前に進みます。
期待しすぎず、でも興味を持ち続ける。
これが、こういう最先端の科学ニュースに対する正しい距離感だと私は思います。
【今後の展開】
このチャンネルでは、ER-100の臨床試験の結果が出たら、もちろんすぐに解説動画を出します。また、セタネオ(セペタプロスト)のような新しい緑内障治療薬の話や、NAIONに対するPrivosegtor(PIONEER試験)の結果など、眼科の最新ニュースも引き続きお届けします。
見逃したくない方は、ぜひチャンネル登録と通知のベルマーク、お願いします。
それでは今日はこの辺で。
眼科医の高橋でした。ありがとうございました。
■ 補足資料:台本内で引用した主要文献
- Lu Y, et al. (2020) "Reprogramming to recover youthful epigenetic information and restore vision." Nature 588:124-129. DOI: 10.1038/s41586-020-2975-4 ※Nature表紙論文
- Takahashi K, Yamanaka S. (2006) "Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors." Cell 126:663-676. ※iPS細胞の原著論文
- Ocampo A, et al. (2016) "In Vivo Amelioration of Age-Associated Hallmarks by Partial Reprogramming." Cell 167:1719-1733. ※部分的リプログラミングのin vivo初報告
- Brenner C. (2023) "A Science-Based Review of the World's Best-Selling Book on Aging." Archives of Gerontology and Geriatrics 107:104894. ※Sinclairの著書Lifespanへの科学的批判
- Life Biosciences プレスリリース (2026年1月28日) "FDA Clearance of IND Application for ER-100 in Optic Neuropathies"
- ClinicalTrials.gov NCT07290244 "Evaluating ER-100 for Safety in People With Glaucoma or NAION"
- Life Biosciences ARDD 2025発表 NHPモデルでのメチル化パターン回復と視機能改善データ
- QPI-1007 Phase 2/3結果 (2025) Ophthalmology 掲載。NAION急性期のsiRNA治療。主要評価項目未達だがサブグループ解析で有意差あり
- Oculis社 PIONEER Program (2025-2026) Privosegtor(SGK-2活性化薬)のNAION向けPhase 3試験(PIONEER-3、2026年半ば開始予定)
■ 台本演出ノート
サムネイル案
- 山中教授とシンクレア教授の顔写真(左右対比)
- 中央にマウス→人間の目のビジュアル
- テキスト:「ノーベル賞の技術で目が若返る!?」「史上初 ヒト臨床試験開始」
テロップ案(要所に表示)
- 「山中因子 = OSKM(Oct4, Sox2, Klf4, c-Myc)」
- 「OSK = c-Mycを除いた3因子」
- 「ER-100 = OSKを発現させるAAVベクター」
- 「Phase 1 = 安全性確認が目的」
- 「結果は早くて2026年末〜2027年初め」
図解・アニメーション案
- DNAメチル化の仕組み(レシピ本+付箋のアニメーション)
- 山中因子4つ → 3つに減らすプロセスの図解
- マウスの視神経再生ビフォーアフター画像(Nature論文のFigureを参考に作画)
- ER-100の投与メカニズムフローチャート
- リプログラミング企業比較表(Altos Labs / Life Bio / YouthBio / Turn Bio)
BGM提案
- 導入部:軽めのシネマティック(好奇心を刺激する感じ)
- 科学解説パート:静かなアンビエント
- シンクレアの「影」パート:やや緊張感のあるトーン
- エンディング:希望感のある明るめの曲